L'IPTG (isopropil-β-D-tiogalattoside) è un analogo del substrato della β-galattosidasi, che è altamente inducibile.Sotto l'induzione di IPTG, l'induttore può formare un complesso con la proteina repressore, in modo che la conformazione della proteina repressore venga modificata, in modo che non possa essere combinata con il gene bersaglio e il gene bersaglio venga espresso in modo efficiente.Quindi come dovrebbe essere determinata la concentrazione di IPTG durante l'esperimento?Più grande è, meglio è?
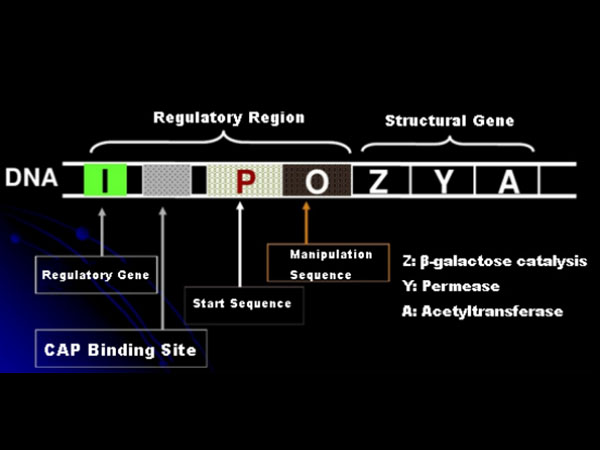
Innanzitutto, comprendiamo il principio di induzione dell'IPTG: l'operone (elemento) del lattosio di E. coli contiene tre geni strutturali, Z, Y e A, che codificano rispettivamente β-galattosidasi, permeasi e acetiltransferasi.lacZ idrolizza il lattosio in glucosio e galattosio o in allo-lattosio;lacY consente al lattosio presente nell'ambiente di passare attraverso la membrana cellulare ed entrare nella cellula;lacA trasferisce il gruppo acetile dall'acetil-CoA al β-galattoside, il che comporta la rimozione dell'effetto tossico.Inoltre, c'è una sequenza operativa O, una sequenza iniziale P e un gene regolatore I. Il codice del gene I è una proteina repressore che può legarsi alla posizione O della sequenza operatore, in modo che l'operone (meta) venga represso e spento.Esiste anche un sito di legame per il sito di legame della proteina CAP dell'attivatore del gene catabolico a monte della sequenza iniziale P. La sequenza P, la sequenza O e il sito di legame della CAP costituiscono insieme la regione regolatrice dell'operone lac.I geni codificanti dei tre enzimi sono regolati dalla stessa regione regolatoria per ottenere l'espressione coordinata dei prodotti genici.
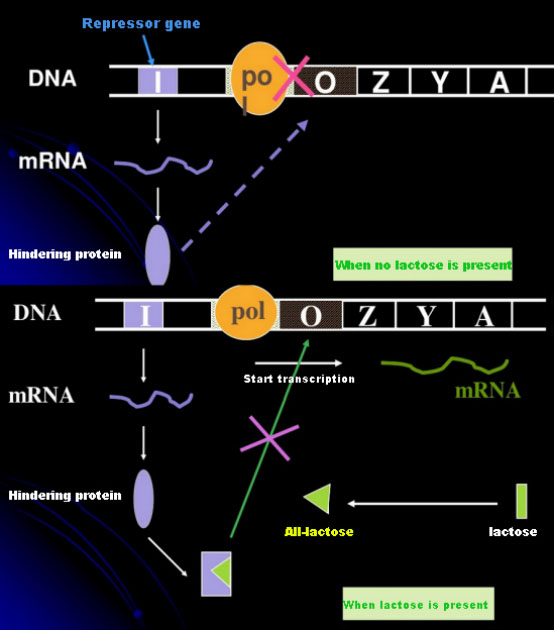
In assenza di lattosio, l'operone lac (meta) è in uno stato di repressione.In questo momento, il repressore lac espresso dalla sequenza I sotto il controllo della sequenza del promotore PI si lega alla sequenza O, che impedisce alla RNA polimerasi di legarsi alla sequenza P e inibisce l'inizio della trascrizione;quando è presente il lattosio, l'operone lac (meta) può essere indotto. In questo sistema dell'operone (meta), il vero induttore non è il lattosio stesso.Il lattosio entra nella cellula e viene catalizzato dalla β-galattosidasi per essere convertito in allolattosio.Quest'ultima, come molecola induttrice, si lega alla proteina repressore e modifica la conformazione della proteina, portando alla dissociazione della proteina repressore dalla sequenza O e alla trascrizione.L'isopropiltiogalattoside (IPTG) ha lo stesso effetto dell'allolattosio.È un induttore molto potente, che non viene metabolizzato dai batteri ed è molto stabile, per questo è ampiamente utilizzato nei laboratori.
Come determinare la concentrazione ottimale di IPTG?Prendiamo come esempio l'Escherichia coli.
Il ceppo geneticamente modificato di E. coli BL21 contenente il pGEX ricombinante positivo (CGRP/msCT) è stato inoculato in terreno liquido LB contenente 50μg·mL-1 Amp e coltivato durante la notte a 37°C.La coltura di cui sopra è stata inoculata in 10 flaconi da 50 ml di terreno liquido LB fresco contenente 50μg·mL-1 Ampere in un rapporto di 1:100 per la coltura di espansione e quando il valore OD600 era 0,6~0,8, IPTG è stato aggiunto alla concentrazione finale.È 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0mmol·L-1.Dopo l'induzione alla stessa temperatura e allo stesso tempo, da essa è stato prelevato 1 mL della soluzione batterica e le cellule batteriche sono state raccolte mediante centrifugazione e sottoposte a SDS-PAGE per analizzare l'influenza delle diverse concentrazioni di IPTG sull'espressione proteica, e poi selezionare la concentrazione di IPTG con la maggiore espressione proteica.
Dopo gli esperimenti, si scoprirà che la concentrazione di IPTG non è la più grande possibile.Questo perché l’IPTG ha una certa tossicità per i batteri.Anche il superamento della concentrazione ucciderà la cellula;e in generale, speriamo che più proteine solubili siano espresse nella cellula, meglio è, ma in molti casi quando la concentrazione di IPTG è troppo alta, si formerà una grande quantità di inclusioni.Corpo, ma la quantità di proteine solubili è diminuita.Pertanto, la concentrazione di IPTG più adatta spesso non è tanto maggiore quanto migliore, ma minore è la concentrazione.
Lo scopo dell'induzione e della coltivazione di ceppi geneticamente modificati è aumentare la resa della proteina bersaglio e ridurre i costi.L'espressione del gene bersaglio non è influenzata solo dai fattori propri del ceppo e dal plasmide di espressione, ma anche da altre condizioni esterne, come la concentrazione dell'induttore, la temperatura di induzione e il tempo di induzione.Pertanto, in generale, prima che una proteina sconosciuta venga espressa e purificata, è meglio studiare il tempo di induzione, la temperatura e la concentrazione di IPTG per selezionare le condizioni appropriate e ottenere i migliori risultati sperimentali.
Orario di pubblicazione: 31 dicembre 2021

